Không đạt chất lượng, thuốc kháng sinh Trimoxtal bị thu hồi trên toàn quốc
Cục quản lý Dược có công văn gửi Sở Y tế các tỉnh, thành phố trực thuộc Trung ương; Công ty cổ phần Dược Minh Hải (Cà Mau) thông báo thu hồi trên toàn quốc thuốc trimoxtal.
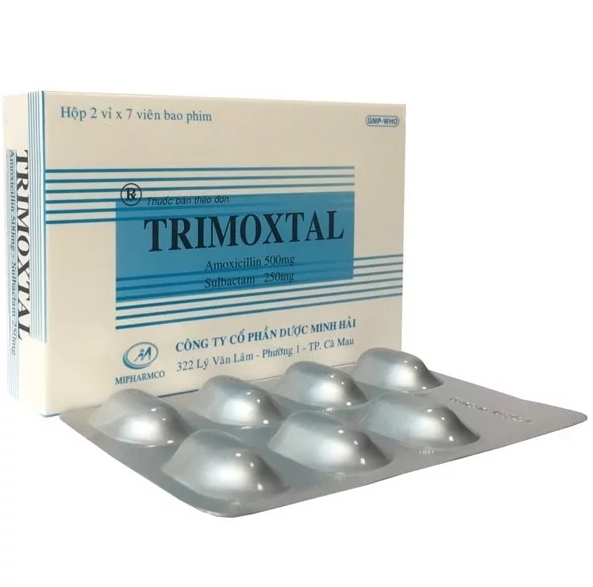
Thu hồi thuốc kháng sinh Trimoxtal trên toàn quốc
Cục Quản lý Dược thông báo thu hồi toàn quốc thuốc viên nén bao phim Trimoxtal 500/250, SĐK: VD20158-13, Số lô: 0040518; NSX: 08/05/2018; HD: 08/05/2021.
Thông tin trên báo Chính phủ, thuốc viên nén bao phim Trimoxtal 500/250 có thành phần có Amoxicilin (dưới dạng Amoxicilin trihydrat) 500 mg; Sulbactam (dưới dạng Sulbactam natri) 250 mg do Công ty cổ phần Dược Minh Hải sản xuất.
Nguyên nhân của việc thu hồi này là qua kiểm nghiệm, mẫu thuốc không đạt tiêu chuẩn chất lượng về chỉ tiêu Định tính Sulbactam natri.
Cục Quản lý Dược yêu cầu sau khi bị thông báo được công bố, Công ty cổ phần Dược Minh Hải phối hợp với nhà phân phối thuốc phải gửi thông báo thu hồi tới các cơ sở bán buôn, bán lẻ, sử dụng Viên nén bao phim Trimoxtal 500/250 và tiến hành thu hồi toàn bộ lô thuốc không đạt tiêu chuẩn chất lượng nêu trên; gửi báo cáo thu hồi về Cục Quản lý Dược trong vòng 18 ngày.
Đồng thời, các đơn vị này phải báo cáo khẩn về tình hình sản xuất và quá trình phân phối lô thuốc viên nén bao phim Trimoxtal 500/250, SĐK: VD-20158-13, Số lô: 0040518 không đạt tiêu chuẩn chất lượng nêu trên.
Rà soát lại hồ sơ đăng ký thuốc, quy trình sản xuất, hồ sơ lô sản xuất, để điều tra xác định nguyên nhân lô thuốc không đạt tiêu chuẩn chất lượng về định tính Sulbactam natri (có sai khác so với hồ sơ đăng ký thuốc) và chỉ tiếp tục sản xuất sản phẩm này sau khi hoàn thành các biện pháp khắc phục phòng ngừa.
Báo cáo khẩn danh sách toàn bộ các lô thuốc Trimoxtal 500/250, SĐK: VD-20158-13 và thông tin về nguyên liệu (tên nguyên liệu, số lô nguyên liệu) đã tiến hành sản xuất, còn hạn dùng và đang lưu hành trên thị trường; tiến hành thu hồi các lô thuốc sử dụng nguyên liệu khác với thành phần công thức đã đăng ký và phê duyệt bởi Cục Quản lý Dược.
Các đơn vị phải gửi báo cáo về Cục Quản lý Dược trước ngày 23/9/2020.